Полезные таблицы по химии 8 класс

«Химия 8 класс. Все формулы и определения»
Ключевые слова: Химия 8 класс. Все формулы и определения, условные обозначения физических величин, единицы измерения, приставки для обозначения единиц измерения, соотношения между единицами, химические формулы, основные определения, кратко, таблицы, схемы.
1. Условные обозначения, названия и единицы измерения
некоторых физических величин, используемых в химии
| Физическая величина | Обозначение | Единица измерения |
| Время | t | с |
| Давление | p | Па, кПа |
| Количество вещества | ν | моль |
| Масса вещества | m | кг, г |
| Массовая доля | ω | Безразмерная |
| Молярная масса | М | кг/моль, г/моль |
| Молярный объем | Vn | м3/моль, л/моль |
| Объем вещества | V | м3, л |
| Объемная доля | | Безразмерная |
| Относительная атомная масса | Ar | Безразмерная |
| Относительная молекулярная масса | Mr | Безразмерная |
| Относительная плотность газа А по газу Б | DБ(А) | Безразмерная |
| Плотность вещества | р | кг/м3, г/см3, г/мл |
| Постоянная Авогадро | NA | 1/моль |
| Температура абсолютная | Т | К (Кельвин) |
| Температура по шкале Цельсия | t | °С (градус Цельсия) |
| Тепловой эффект химической реакции | Q | кДж/моль |

2. Соотношения между единицами физических величин



3. Химические формулы в 8 классе

Схема. Химические формулы в 8 классе
4. Основные определения в 8 классе

- Атом — мельчайшая химически неделимая частица вещества.
- Химический элемент — определённый вид атомов.
- Молекула — мельчайшая частица вещества, сохраняющая его состав и химические свойства и состоящая из атомов.
- Простые вещества — вещества, молекулы которых состоят из атомов одного вида.
- Сложные вещества — вещества, молекулы которых состоят из атомов разного вида.
- Качественный состав вещества показывает, из атомов каких элементов оно состоит.
- Количественный состав вещества показывает число атомов каждого элемента в его составе.
- Химическая формула — условная запись качественного и количественного состава вещества посредством химических символов и индексов.
- Атомная единица массы (а.е.м.) — единица измерения массы атома, равная массы 1/12 атома углерода 12С.
- Моль — количество вещества, в котором содержится число частиц, равное числу атомов в 0,012 кг углерода 12С.
- Постоянная Авогадро (Na = 6*1023 моль-1) — число частиц, содержащихся в одном моле.
- Молярная масса вещества (М) — масса вещества, взятого в количестве 1 моль.
- Относительная атомная масса элемента Аr — отношение массы атома данного элемента m0 к 1/12 массы атома углерода 12С.
- Относительная молекулярная масса вещества Мr — отношение массы молекулы данного вещества к 1/12 массы атома углерода 12С. Относительная молекулярная масса равна сумме относительных атомных масс химических элементов, образующих соединение, с учётом числа атомов данного элемента.
- Массовая доля химического элемента ω(Х) показывает, какая часть относительной молекулярной массы вещества X приходится на данный элемент.
АТОМНО-МОЛЕКУЛЯРНОЕ УЧЕНИЕ
1. Существуют вещества с молекулярным и немолекулярным строением.
2. Между молекулами имеются промежутки, размеры которых зависят от агрегатного состояния вещества и температуры.
3. Молекулы находятся в непрерывном движении.
4. Молекулы состоят из атомов.
6. Атомы характеризуются определённой массой и размерами.
При физических явлениях молекулы сохраняются, при химических, как правило, разрушаются. Атомы при химических явлениях перегруппировываются, образуя молекулы новых веществ.

ЗАКОН ПОСТОЯНСТВА СОСТАВА ВЕЩЕСТВА
Каждое химически чистое вещество молекулярного строения независимо от способа получения имеет постоянный качественный и количественный состав.
ВАЛЕНТНОСТЬ
Валентность — свойство атома химического элемента присоединять или замещать определённое число атомов другого элемента.

ХИМИЧЕСКАЯ РЕАКЦИЯ
Химическая реакция — явление, в результате которого из одних веществ образуются другие. Реагенты — вещества, вступающие в химическую реакцию. Продукты реакции — вещества, образующиеся в результате реакции.
Признаки химических реакций:
1. Выделение теплоты (света).
2. Изменение окраски.
3. Появление запаха.
4. Образование осадка.
5. Выделение газа.
- Химическое уравнение — запись химической реакции с помощью химических формул. Показывает, какие вещества и в каком количестве вступают в реакцию и получаются в результате реакции.
ЗАКОН СОХРАНЕНИЯ МАССЫ ВЕЩЕСТВ
Масса веществ, вступивших в химическую реакцию, равна массе веществ, образовавшихся в результате реакции. В результате химических реакций атомы не исчезают и не возникают, а происходит их перегруппировка.
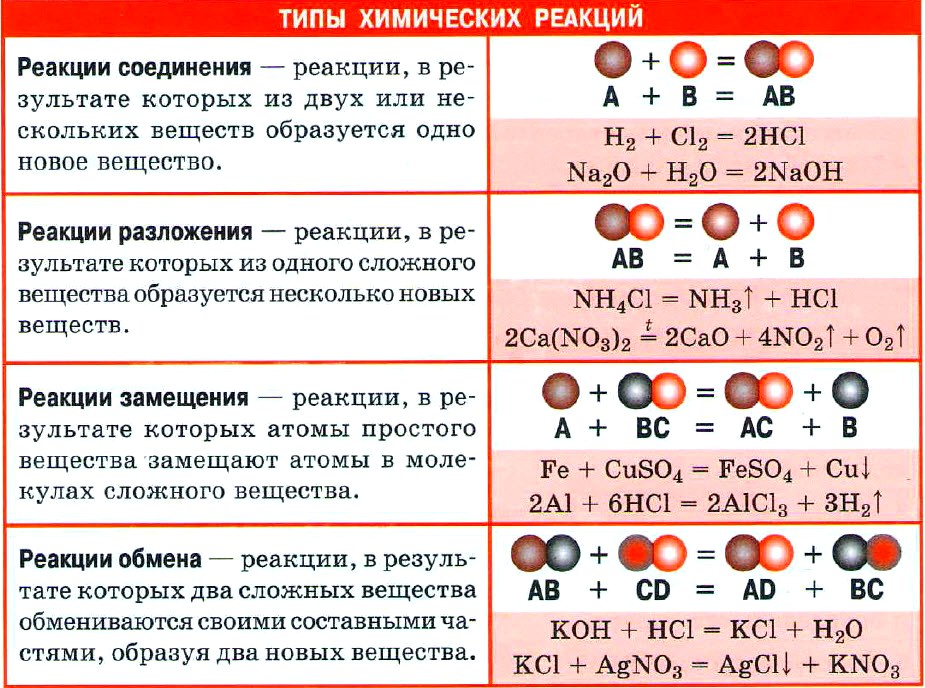
Важнейшие классы неорганических веществ

Воздух. Кислород. Горение

Конспект урока «Химия 8 класс. Все формулы и определения».
Следующая тема: «».
Источник
“Единственный путь, ведущий к знаниям, – это деятельность”.
(Бернард Шоу)
Пусть зимний день с метелями
Мне навевает грусть.
Таблицу Менделеева
Я знаю наизусть!
Динамическая таблица Менделеева
Игра “Таблица Менделеева” – жми на картинку и играй!
Таблица с русскими и латинскими названиями химических элементов
ХЭ таблица.png
Portable Network Image Format
9.3 KB
Естественные семейства элементов
Зависимость свойств элементов от атомног
JPG Image
135.2 KB
Примеры составления молекулярных и структурных формул
Составление структурных формул 8 кл.gif
Graphic Interchange format
12.5 KB
Правила определения валентности
РАЗДАТОЧНЫЙ валентность 8 класс.doc
Microsoft Word Document
35.5 KB
Изменение цвета индикаторов в различных средах
Изменение окраски кислотно-основных инди
Microsoft Word Document
39.5 KB
Таблица растворимости
Таблица растворимости солей, кислот и ос
Microsoft Word Document
43.0 KB
Важнейшие классы неорганических соединений
Опорный конспект Классы неорган соед.doc
Microsoft Word Document
92.5 KB
Таблица с названиями кислот и их кислотных остатков
кислоты и остатки.doc
Microsoft Word Document
59.0 KB
Оксиды и соответствующие им гидроксиды
Раздаточный ОКСИДЫ 8 класс.doc
Microsoft Word Document
87.0 KB
Опорная схема Генетическая связь между классами неорганических соединений
Генетическая связь.jpg
JPG Image
110.5 KB
Опорная схема “Оксиды”
ОС Оксиды 8 кл.docx
Microsoft Word Document
88.0 KB
Опорная схема “Основания”
ОС Основания 8 кл.docx
Microsoft Word Document
76.5 KB
Опорная схема “Кислоты”
ОС Кислоты 8 кл.docx
Microsoft Word Document
60.1 KB
Определение степеней окисления
1.png
Portable Network Image Format
431.7 KB
Составление формул по с/о
2.png
Portable Network Image Format
383.1 KB
Опорная схема “П/гр Азота”
ОС пгр Азота.docx
Microsoft Word Document
81.8 KB
Опорная схема “Азот”
ОС Азот простое вещество.docx
Microsoft Word Document
62.9 KB
Опорная схема “Аммиак”
ОС Аммиак.docx
Microsoft Word Document
51.2 KB
ЭХ ряд активности металлов, таблица и закономерности
ПАМЯТКА ЭХ ряд Ме.doc
Microsoft Word Document
74.0 KB
ОЭО
Относительные электроотрицательности эле
Microsoft Word Document
43.5 KB
Металлы
доп мат-л по Ме.doc
Microsoft Word Document
2.0 MB
Тривиальные названия некоторых веществ
Кислоты и их кислотные остатки
Экзамен по химии за 10 класс
Экзамен ХИМИЯ за 10 класс.doc
Microsoft Word Document
58.5 KB
ВАЖНЕЙШИЕ альфа АМИНОКИСЛОТЫ.doc
Microsoft Word Document
44.0 KB
Онлайн тест для учащихся 10 и 11 класса
Интерактивный мультимедиа учебник по органической химии
Химия в таблицах и схемах 1
Хим в табл и сх1.zip
Compressed Archive in ZIP Format
1.3 MB
Химия в таблицах и схемах 2
Хим в табл и сх2.zip
Compressed Archive in ZIP Format
1.5 MB
Химия в таблицах и схемах
Хим в табл и сх1.zip
Compressed Archive in ZIP Format
1.3 MB
Краткая характеристика самостоятельных работ учащихся
Виды самостоятельных работ.docx
Microsoft Word Document
13.0 KB
Требования к оформлению реферата
Требования к оформлению реферата.doc
Microsoft Word Document
40.5 KB
Требования к оформлению презентаций
Требования к презентациям.doc
Microsoft Word Document
235.0 KB
Источник
Химия в таблицах и схемах. 8 класс. Данное пособие отражает в сжатой и наглядной форме все основные разделы курса химии 8 класса, оформленные в виде таблиц и схем. Пособие может быть использовано учащимися для закрепления на уроках и при выполнении домашних заданий.
Настоящее пособие может дополнить любой учебник химии для 8 класса общеобразовательной школы.
Химия в таблицах и схемах. 8 класс. Ковалевская Н.Б.
Описание учебника
Содержание
1. ПЕРВОНАЧАЛЬНЫЕ ХИМИЧЕСКИЕ ПОНЯТИЯ
1.1 Вещество. Свойства веществ 3
1.2 Молекулы и атомы. Атомно-молекулярное учение 4
1.3 Чистые вещества и смеси. Способы разделения смесей 5
1.4 Физические и химические явления 6
1.5 Химический элемент 7
1.6 Химические символы (Знаки химических элементов) 8
1.7 Знакомство с символами и названиями элементов 9
1.8 Простые и сложные вещества. Аллотропия 10
1.9 Химические формулы 11
2. КОЛИЧЕСТВЕННЫЕ ОТНОШЕНИЯ В ХИМИИ
2.1 Относительная атомная масса 12
2.2 Относительная молекулярная масса 13
2.3 Закон постоянства состава 14
2.4 Массовые отношения 15
2.5 Массовая доля элемента 16
ЧИСТЫЕ ВЕЩЕСТВА И СМЕСИ. СПОСОБЫ РАЗДЕЛЕНИЯ СМЕСЕЙ
Чистыми называются вещества, состоящие из одинаковых молекул. Смесь состоит из молекул разных веществ.
Однородными называются смеси, в которых даже с помощью микроскопа нельзя обнаружить частицы веществ, входящих в смесь.
Неоднородными называются смеси, в которых невооруженным глазом или с помощью микроскопа можно заметить частицы веществ,составляющие смесь.
В смеси сохраняются свойства составляющих их веществ компонентов.
На основании этих свойств выбирают рациональный способ разделения смесей.
ФИЗИЧЕСКИЕ И ХИМИЧЕСКИЕ ЯВЛЕНИЯ
Явления
физические
1. Тесное соприкосновение (необходимо)
2. Нагревание (возможно):
а) для начала реакции
б)постоянно
химические
1. Изменение цвета;
2. Изменение запаха;
3. Выпадение (растворение) осадка;
4. Выделение газа;
5. Выделение (поглощение) теплоты (иногда света).
Условия течения Признаки
химических реакций: химических реакций:
ХИМИЧЕСКИЙ ЭЛЕМЕНТ
Элемент (стихия, первоначальное вещество) составная часть сложного целого.
Советский энциклопедический словарь.
Элементарный. Начальный, относящийся к основам чего-либо.
Ожегов С.И. Словарь русского языка.
Химический элемент составная часть вещества.
Роберт Бойль
Химический элемент это определенный вид атомов.
Джон Дальтон
Химический элемент — это вид атомов, арактеризующийся определенным зарядом ядра, строением электронных оболочек. Число элементов ограничено, а их комбинации дают все многообразие веществ.
В природе (на Земле) установлено существование 89 различных химических элементов. Некоторые элементы получены искусственным путем с использованием ядерных реакторов. В настоящее время известно 110 хим. элементов.
«Вся сущность теоретического учения в химии лежит в отвлеченном понятии об элементах. Найти их свойства,определить причины их различия и сходства, а потом, на основании этого, предугадать свойства образуемых ими тел вот путь, по которому идет эта наука…
Д.И.Менделеев
Аллотропия — это явление образования химическим элементом нескольких простых веществ, различных по строению и свойствам. Образующиеся вещества называются аллотропными видоизменениями.
С — алмаз, графит, карбин; О кислород, озон; Р белый, красный, черный; 5 ромбическая, моноклинная, пластическая
Химическая формула — это условная запись состава вещества посредством химических знаков и индексов. (Индекс — цифра, стоящая справа внизу от символа. Обозначает число атомов в молекуле)
МАССОВАЯ ДОЛЯ ЭЛЕМЕНТА
Массовая
доля элемента —
физическая величина, которая
показывает, какую часть (долю) составляет масса данного элемента от всей массы вещества
измеряется в долях, %
СО (Э) массовая доля элемента
П — число атомов Аг(Э) — относительная атомная масса элемента Мг — относительная молекулярная масса веществаСОСТАВЛЕНИЕ ХИМИЧЕСКИХ ФОРМУЛ БИНАРНЫХ СОЕДИНЕНИЙ (ПО ВАЛЕНТНОСТИ ЭЛЕМЕНТОВ)
Алгоритм решения Пример
1. Запишите символы элементов (согласно ряду электроотрицательности).
2. Запишите валентности элементов (по периодической системе).
3. Найдите наименьшее общее кратное (н.о.к.) между числовыми значениями валентности.
4. Найдите отношение между атомами элементов (деля н.о.к. на соответствующую валентность). Полученные числа являются индексами.
5. Запишите формулу вещества.
ХИМИЧЕСКОЕ УРАВНЕНИЕ
Химическим уравнением называют условную
запись химической реакции посредством химических формул и математических знаков.
Оно показывает, какие вещества и в каких количествах вступили и получились в результате химической реакции.
В уравнениях химических реакций число атомов каждого элемента слева и справа от знака равенства должно быть одинаково.
ХИМИЧЕСКИЕ УРАВНЕНИЯ
Алгоритм составления химического уравнения
Уравнение химической реакции между водородом и кислородом
1. Составить схему взаимодействия: слева записать формулы веществ, вступивших в реакцию, справа получившихся, соединив их знаком. В реакцию вступают 2 простых вещества,получается 1 сложное вещество.
Предложения интернет-магазинов
Источник



Д.И. Менделеева расширенная и доработанная
(атомная масса, электронное строение, электро-отрицательность, температура плавления,
температура кипения)
и оснований в воде
и оснований в воде



и гомолог
в различных средах


Электрохимический ряд напряжений металлов

Плотность и температура плавления металлов



и их молекулярные или формульные массы
Электрохимический ряд напряжений металлов
Ряд электроотрицательности неметаллов (2 x 0.45 m)



углеводородов
неорганических соединений
солей и оснований
 |  |  |  |
| Углеводороды | Органические соединения | Решение задач по химическим уравнениям | Физические величины, используемые при решении задач |
 |  |  |  |
| Алгоритм описания свойств элемента по положению в периодической системе | Алгоритм описания реакции | Алгоритм характеристики вещества | Относительные электроотрицательности элементов |
 |  |  |  |
| Химические знаки и округленные атомные массы важнейших элементов | Принцип электронного строения атомов химических элементов | Стандартные электродные потенциалы материалов | Выполняйте опыты только по инструкции |
 |  |  |  |
| Классификация химических реакций | Химическая связь | Строение атома | Перенапряжение выделения водорода и ионизации кислорода при плотности тока 1 мА/см2 на различных металлах |



некоторых комплексных ионов
и некоторых cлабых кислот
и оснований в водных растворах



потенциалы металлов
в различных средах, В
на уроке химии
 |  |  |  |
| Плотность растворов кислот, щелочей и солей различных концентраций при 15° C | Произведение растворимости малорастворимых в воде электролитов при 25°с | Электрохимические системы Электроды первого рода, обратимые относительно катиона | Качественные реакции на катионы и анионы |

(Комплект из трёх таблиц)



Углеводороды



ряд электроотрицательности элементов, электрохимический ряд напряжения металлов
Источник
