Что за полезное ископаемое радиоактивный металл

Главная » Металлы » Виды и характеристики радиоактивных металлов
На чтение 5 мин.
Радиоактивные металлы занимают значительную часть периодической таблицы Менделеева. Одни о них говорят со страхом, другие с интересом. Данные элементы обладают уникальными свойствами, за которые ценятся научным сообществом, но вредны для человека. Излучение, которое исходит от этих металлов, провоцирует разрушение внутренних органов.
 Химические элементы
Химические элементы
Какие элементы относятся к радиоактивным?
Группа радиоактивных элементов в периодической таблице Менделеева начинается от свинца и заканчивается последней ячейкой. Излучение происходит из-за определенного периода полураспада — преобразования металлического ядра в дочернее. Радиоактивные элементы:
- уран;
- плутоний;
- радий;
- берклий;
- торий;
- нептуний;
- франций;
- эйнштейний;
- технeций.
Среди них присутствуют цветные и черные радиоактивные металлы.
Существуют три вида радиоактивного излучения — альфа, бета, гамма. Они отличаются длиной волны, проникающей способностью. Если альфа излучение может сдержать плотная бумага или картон, то гамма излучение остановит только слой свинца.
Химический элемент нептуний (Фото: Instagram / amurasoap)
История открытия
Открытием радиации человечество обязано прусскому физику Вильгельму Рентгену. В 1895 году он смог увидеть радиоактивное излучение. Благодаря работам этого ученого был разработан рентгеновский аппарат.
Изучение радиоактивности продолжил Анри Беккерель в 1896 году. Этот ученый проводил эксперименты с солями урана. Прорыв в данной области произошел через 2 года. Пьер Кюри получил первый чистый радиоактивный материал — радий. После открытия этого элемента ученый не смог продолжить его изучение, поскольку умер от излучения.
Следующее продвижение в этой области произошло в 1934 году. В этот год ученые смогли синтезировать искусственный радиоактивный изотоп. Сейчас эта область является одной из самых актуальных. Ее изучением занято огромное количество ученых, крупных научных организаций.
Запасы и месторождения
Запасы и месторождения представителей радиоактивной группы:
- Уран. Залежи металла в слоях литосферы на толщину 20 км — 1.3х1014 т. Содержание в морской воде — 3 мкг/л. Больше всего урана содержится в кислых породах, содержащих кремний.
- Радий. Редкий элемент. За все время было добыто не более 1,5 килограмма чистого радия. Природный радий появляется после распада урана 235 и урана 238.
- Плутоний. Из-за отсутствия стабильных изотопов его сложно найти в природе. Изотопы, с длительным периодом полураспада — 239, 244. В природе он встречается в виде соединения PuO2. Его добыча не имеет смысла из-за малого количества.
- Торий. Был открыт в 1815 году. Все природные изотопы элемента состоят из этого нуклида. В большом количестве содержится в природе. Самые стабильные изотопы — 232, 230, 229.
- Берклий. Некоторые изотопы этого радиоактивного элемента можно получить при облучении урановых, плутониевых руд в ядерных реакторах. Самые стабильные изотопы — 247, 249.
Большинство радиоактивных металлов редко встречаются в природе, добывать их сложно.
Добыча руды (Фото: Instagram / nornickel_official)
Добыча и промышленное получение
В чистом виде естественные радиоактивные металлы найти невозможно. Чаще их синтезируют из урановых руд. Это затратный, трудоемкий процесс, состоящий из нескольких этапов:
- Концентрирование. Руду дробят в воде для выделения осадка.
- Выщелачивание. Осадок переводится в раствор.
- Выделение чистого урана.
- Перевод в твердое состояние.
После обработки из тонны руды получается несколько грамм чистого вещества. Проводить подобные процедуры можно только в специальных цехах.
Свойства и характеристики
Знание характеристик радиоактивных металлов поможет выявить уникальные свойства этих элементов, понять, где их лучше применять.
Уран
Свойства:
- В свободном состоянии — светло-серый металл.
- Плотность — 18700 кг/м3.
- Атомный номер — 92.
- Электросопротивление — 29,0•10-4 (Ом•м).
- Температура плавления — 1135°C.
- Теплоемкость — 27,66 Дж/(моль•К).
- Температура кипения — 3818°C.
- Теплопроводность — 22,5 Вт/(м•К).
- Степень окисления — до +6.
- Коэффициент линейного расширения — 10,7•10-6 К-1.
Уран растворяется в азотной и соляной кислоте, не взаимодействует с щелочами. При нагревании может вступать в реакции с азотом, фосфором.
 Химический элемент уран
Химический элемент уран
Радий
Характеристики:
- В нормальном состоянии — серебристо-белый металл.
- Показатель плотности — 5500 кг/м3.
- Атомный номер — 88.
- Показатель теплоемкости — Cp0 29 Дж/(моль•К).
- Температура плавления — 969°C.
- Степень окисления — +2.
- Температура кипения — 1500°C.
По химической активности радий можно сравнить с барием. На воздухе быстро окисляется. При соединении с водой возникает бурная реакция с нагреванием жидкости.
Плутоний
Характеристики:
- При нормальном состоянии — серебристо-белый металл.
- Показатель плотности — 19,82 (25°C, г/см3).
- Атомный норме — 94.
- Удельное электрическое сопротивление — 150 мкОм·см (при +22 °C).
- Температура плавления — 640°C.
- Температура кипения — 3235°C.
Вступает в реакцию с водой.
Окисленный плутоний (Фото: Instagram / thoisoi)
Сферы применения
Радиоактивные металлы применяются в разных направлениях. С их помощью проводят эксперименты, изучают влияние на другие материалы, живые организмы. Часто используются для выработки энергии в реакторах.
Влияние на организм
Радиоактивное излучение разрушает внутренние органы. Естественные механизмы защиты организма справляются только с малыми дозами излучения. Когда они становятся большими, развивается лучевая болезнь, повышается риск поражения организма раком.
Радиоактивные металлы обладают уникальными свойствами. Их изучением ученые занимаются постоянно. Исследователи находят новые способы получения металлов, сферы для их применения.
Источник
Среди всех элементов периодической системы значительная часть принадлежит таким, о которых большинство людей говорят со страхом. А как же иначе? Ведь они являются радиоактивными, а это означает прямую угрозу здоровью людей.
Попробуем разобраться, какие же именно элементы являются опасными, и что они собой представляют, а также выясним, в чем заключается их вредоносное действие на организм человека.

Общее понятие о группе радиоактивных элементов
В данную группу входят металлы. Их достаточно много, располагаются они в периодической системе сразу после свинца и до самой последней ячейки. Главный критерий, по которому принято относить тот или иной элемент к группе радиоактивных, – это его способность обладать определенным периодом полураспада.
Другими словами, радиоактивный распад – это преобразование ядра металла в другое, дочернее, которое сопровождается испусканием излучения определенного вида. При этом происходят превращения одних элементов в другие.
Радиоактивный металл – это тот, у которого хотя бы один изотоп является таковым. Даже если всего разновидностей будет шесть, и при этом лишь одна из них будет носителем данного свойства, весь элемент станет считаться радиоактивным.
Виды излучений
Основными вариантами излучения, которое испускается металлами при распадах, являются:
- альфа-частицы;
- бета-частицы или нейтринный распад;
- изомерный переход (гамма-лучи).
Есть два варианта существования подобных элементов. Первый – это естественный, то есть когда радиоактивный металл встречается в природе и самым простым путем под влиянием внешних сил с течением времени преобразуется в иные формы (проявляет свою радиоактивность и распадается).

Вторая группа – это искусственно созданные учеными металлы, способные к быстрому распаду и мощному выделению большого количества радиационного излучения. Делается это для использования в определенных сферах деятельности. Установки, в которых производятся ядерные реакции по превращениям одних элементов в другие, называются синхрофазотронами.
Разница между двумя обозначенными способами полураспада очевидна: в обоих случаях он самопроизвольный, однако лишь искусственно полученные металлы дают именно ядерные реакции в процессе деструктуризации.
Основы обозначения подобных атомов
Так как у большей части элементов лишь один или два изотопа являются радиоактивными, принято указывать конкретный вид при обозначениях, а не весь элемент в целом. Например, свинец – это просто вещество. Если же принимать во внимание, что он – радиоактивный металл, то следует называть его, например, “свинец-207”.
Периоды полураспада рассматриваемых частиц могут сильно варьироваться. Есть изотопы, которые существуют лишь 0,032 секунды. Но наравне с ними встречаются и те, что распадаются миллионы лет в земных недрах.
Радиоактивные металлы: список
Полный перечень всех принадлежащих к рассматриваемой группе элементов может быть достаточно внушительным, ведь всего к ней относятся около 80 металлов. В первую очередь это все, стоящие в периодической системе после свинца, включая группу лантаноидов и актиноидов. То есть висмут, полоний, астат, радон, франций, радий, резерфордий и так далее по порядковым номерам.

Выше обозначенной границы располагается множество представителей, каждый из которых также имеет изотопы. При этом некоторые из них могут быть как раз радиоактивными. Поэтому важно, какие разновидности имеет химический элемент. Радиоактивный металл, точнее одна из его изотопных разновидностей, есть практически у каждого представителя таблицы. Например, их имеют:
- кальций;
- селен;
- гафний;
- вольфрам;
- осмий;
- висмут;
- индий;
- калий;
- рубидий;
- цирконий;
- европий;
- радий и другие.
Таким образом, очевидно, что элементов, проявляющих свойства радиоактивности, очень много – подавляющее большинство. Часть из них безопасна из-за слишком длинного периода полураспада и содержится в природе, другая же создана искусственно человеком для различных нужд в науке и технике и является крайне опасной для организма людей.
Характеристика радия
Название элементу дано его первооткрывателями – супругами Кюри, Пьером и Марией. Именно эти люди впервые обнаружили, что один из изотопов этого металла – радий-226 – это наиболее устойчивая форма, обладающая особыми свойствами радиоактивности. Это произошло в 1898 году, и о подобном явлении только стало известно. Подробным его изучением как раз и занялись супруги химики.
Этимология слова берет корни из французского языка, на котором оно звучит как radium. Всего известно 14 изотопных модификаций данного элемента. Но наиболее устойчивые формы с массовыми числами:
- 220;
- 223;
- 224;
- 226;
- 228.
Ярко выраженной радиоактивностью обладает форма 226. Сам по себе радий – химический элемент под номером 88. Атомная масса [226]. Как простое вещество способен к существованию. Представляет собой серебристо-белый радиоактивный металл с температурой плавления около 6700С.

С химической точки зрения проявляет достаточно высокую степень активности и способен реагировать с:
- водой;
- органическими кислотами, формируя устойчивые комплексы;
- кислородом, образуя оксид.
Свойства и применение
Также радий – химический элемент, который формирует ряд солей. Известны его нитриды, хлориды, сульфаты, нитраты, карбонаты, фосфаты, хроматы. Также есть двойные соли с вольфрамом и бериллием.
То, что радий-226 может быть опасен для здоровья, его первооткрыватель Пьер Кюри узнал не сразу. Однако сумел убедиться в этом, когда провел эксперимент: сутки он ходил с привязанной к плечевой части руки пробиркой с металлом. На месте контакта с кожей появилась незаживающая язва, избавиться от которой ученый не мог больше двух месяцев. От своих экспериментов над явлением радиоактивности супруги не отказались, поэтому и умерли оба от большой дозы облучения.
Помимо отрицательного значения, существует и ряд областей, в которых радий-226 находит применение и приносит пользу:
- Индикатор смещения уровня океанских вод.
- Используется для определения количества урана в породе.
- Входит в состав осветительных смесей.
- В медицине используется для формирования лечебных радоновых ванн.
- Применяют с целью снятия электрических зарядов.
- С его помощью проводится дефектоскопия литья и свариваются швы деталей.
Плутоний и его изотопы
Данный элемент был открыт в сороковых годах XX века американскими учеными. Впервые его выделили из урановой руды, в которой он сформировался из нептуния. Последний при этом – результат распада уранового ядра. То есть все они между собой тесно взаимосвязаны общими радиоактивными превращениями.

Существует несколько устойчивых изотопов данного металла. Однако наиболее распространенной и важной практически разновидностью является плутоний-239. Известны химические реакции данного металла с:
- кислородом,
- кислотами;
- водой;
- щелочами;
- галогенами.
По своим физическим свойствам плутоний-239 является хрупким металлом с температурой плавления 6400С. Основные способы воздействия на организм – это постепенное формирование онкологических заболеваний, накапливание в костях и вызывание их разрушения, заболевания легких.
Область использования – в основном ядерная промышленность. Известно, что при распаде одного грамма плутония-239 выделяется такое количество теплоты, которое сравнимо с 4-мя тоннами сгоревшего угля. Именно поэтому этот вид металла находит такое широкое применение в реакциях. Ядерный плутоний – источник энергии в атомных реакторах и термоядерных бомбах. Он же используется при изготовлении электрических аккумуляторов энергии, срок службы которых может достигать пяти лет.
Уран – источник радиации
Данный элемент был открыт в 1789 году химиком из Германии Клапротом. Однако исследовать его свойства и научиться применять их на практике люди сумели лишь в XX веке. Основная отличительная особенность в том, что радиоактивный уран способен при естественном распаде образовывать ядра:
- свинца-206;
- криптона;
- плутония-239;
- свинца-207;
- ксенона.
В природе этот металл светло-серого цвета, обладает температурой плавления свыше 11000С. Встречается в составе минералов:
- Урановые слюдки.
- Уранинит.
- Настуран.
- Отенит.
- Тюянмунит.
Известны три стабильных природных изотопа и 11 искусственно синтезированных, с массовыми числами от 227 до 240.

В промышленности широко используется радиоактивный уран, способный быстро распадаться с высвобождением энергии. Так, его используют:
- в геохимии;
- горном деле;
- ядерных реакторах;
- при изготовлении ядерного оружия.
Влияние на организм человека ничем не отличается от предыдущих рассмотренных металлов – накопление приводит к повышенной дозе облучения и возникновению раковых опухолей.
Трансурановые элементы
Самыми главными из металлов, стоящих вслед за ураном в периодической системе, являются те, что были открыты совсем недавно. Буквально в 2004 году в свет вышли источники, подтверждающие рождение на свет 115 элемента периодической системы.
Им стал самый радиоактивный металл из всех известных на сегодняшний день – унунпентий (Uup). Его свойства остаются не изученными до сих пор, ведь период полураспада составляет 0,032 секунды! Рассмотреть и выявить подробности строения и проявляемые особенности при таких условиях просто невозможно.
Однако его радиоактивность во много раз превосходит показатели второго по данному свойству элемента – плутония. Тем не менее используется на практике не унунпентий, а более “медленные” его товарищи по таблице – уран, плутоний, нептуний, полоний и прочие.
Еще один элемент – унбибий – теоретически существует, однако доказать это практически ученые разных стран не могут с 1974 года. Последняя попытка была совершена в 2005 году, однако оказалась не подтвержденной общим советом ученых-химиков.
Торий
Был открыт еще в XIX веке Берцелиусом и назван в честь скандинавского бога Тора. Является слаборадиоактивным металлом. Такой особенностью обладают пять из его 11-ти изотопов.
Основное применение в ядерной энергетике основано не на способности испускать огромное количество тепловой энергии при распаде. Особенность в том, что ядра тория способны захватывать нейтроны и превращаться в уран-238 и плутоний-239, которые уже и вступают непосредственно в ядерные реакции. Поэтому и торий можно отнести к группе рассматриваемых нами металлов.

Полоний
Серебристо-белый радиоактивный металл под номером 84 в периодической системе. Открыт был все теми же ярыми исследователями радиоактивности и всего, что с ней связано, супругами Марией и Пьером Кюри в 1898 году. Главная особенность этого вещества в том, что оно свободно существует около 138,5 дней. То есть таков период полураспада данного металла.
В природе встречается в составе урановых и других руд. Используется как источник энергии, причем достаточно мощной. Является стратегическим металлом, так как применяется для изготовления ядерного оружия. Количество строго ограничено и находится под контролем каждого государства.
Также используется для ионизации воздуха, устранения статического электричества в помещении, при изготовлении космических обогревателей и прочих схожих предметов.
Воздействие на организм человека
Все радиоактивные металлы обладают способностью проникать сквозь кожу человека и накапливаться внутри организма. Они очень плохо выводятся с продуктами жизнедеятельности, вообще не выводятся с потом.
Со временем начинают поражать дыхательную, кровеносную, нервную системы, вызывая в них необратимые изменения. Воздействуют на клетки, заставляя их функционировать неправильно. В результате происходит образование злокачественных опухолей, возникают онкологические заболевания.
Поэтому каждый радиоактивный металл – большая опасность для человека, особенно если говорить о них в чистом виде. Нельзя трогать их незащищенными руками и находиться в помещении вместе с ними без специальных защитных приспособлений.
Источник
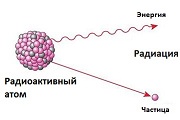
Радиоактивные металлы — это металлы, которые самопроизвольно излучают поток элементарных частиц во внешнюю среду. Этот процесс называют альфа(α), бета(β), гамма(γ) излучением или просто радиоактивным излучением.
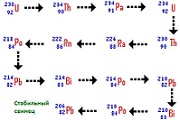
Все радиоактивные металлы со временем распадаются и превращаются в стабильные элементы (иногда проходя целую цепочку превращений). У разных элементов радиоактивный распад может длиться от нескольких миллисекунд до нескольких тысяч лет.
Рядом с названием радиоактивного элемента часто указывается массовое число его изотопа. Например, Технеций-91 или 91Tc. Разные изотопы одного и того же элемента как правило имеют общие физические свойства и различаются лишь длительностью радиоактивного распада.

Список радиоактивных металлов
| Название рус. | Название eng. | Самый стабильный изотоп | Период распада |
|---|---|---|---|
| Технеций | Technetium | Tc-91 | 4.21 x 106 лет |
| Прометий | Promethium | Pm-145 | 17.4 года |
| Полоний | Polonium | Po-209 | 102 года |
| Астат | Astatine | At-210 | 8.1 часов |
| Франций | Francium | Fr-223 | 22 минут |
| Радий | Radium | Ra-226 | 1600 лет |
| Актиний | Actinium | Ac-227 | 21.77 лет |
| Торий | Thorium | Th-229 | 7.54 x 104 лет |
| Протактиний | Protactinium | Pa-231 | 3.28 x 104 лет |
| Уран | Uranium | U-236 | 2.34 x 107 лет |
| Нептуний | Neptunium | Np-237 | 2.14 x 106 лет |
| Плутоний | Plutonium | Pu-244 | 8.00 x 107 лет |
| Америций | Americium | Am-243 | 7370 лет |
| Кюрий | Curium | Cm-247 | 1.56 x 107 лет |
| Беркелий | Berkelium | Bk-247 | 1380 лет |
| Калифорний | Californium | Cf-251 | 898 лет |
| Эйнштейний | Einsteinium | Es-252 | 471.7 дней |
| Фермий | Fermium | Fm-257 | 100.5 дней |
| Менделевий | Mendelevium | Md-258 | 51.5 дней |
| Нобелий | Nobelium | No-259 | 58 минут |
| Лоуренсий | Lawrencium | Lr-262 | 4 часа |
| Резенфордий | Rutherfordium | Rf-265 | 13 часов |
| Дубний | Dubnium | Db-268 | 32 часа |
| Сиборгий | Seaborgium | Sg-271 | 2.4 минуты |
| Борий | Bohrium | Bh-267 | 17 секунд |
| Ганий | Hassium | Hs-269 | 9.7 секунд |
| Мейтнерий | Meitnerium | Mt-276 | 0.72 секунды |
| Дармштадий | Darmstadtium | Ds-281 | 11.1 секунды |
| Рентгений | Roentgenium | Rg-281 | 26 секунд |
| Коперниций | Copernicium | Cn-285 | 29 секунд |
| Унунтрий | Ununtrium | Uut-284 | 0.48 секунд |
| Флеровий | Flerovium | Fl-289 | 2.65 секунд |
| Унунпентий | Ununpentium | Uup-289 | 87 миллисекунд |
| Ливерморий | Livermorium | Lv-293 | 61 миллисекунда |
Радиоактивные элементы делятся на естественные (существующие в природе) и искусственные (получаемые в результате лабораторного синтеза). Естественных радиоактивных металлов не много — это полоний, радий, актиний, торий, протактиний и уран. Их наиболее стабильные изотопы встречаются в природе, чаще в виде руды. Все остальные металлы из списка созданы человеком.
Самый радиоактивный металл
Самый радиоактивный металл на данный момент — ливерморий. Его изотоп Ливерморий-293 распадается всего за 61 милисекунду. Впервые этот изотоп был получен в Дубне, в 2000 году.
Другой очень радиоактивный металл — унунпентий. Изотоп унунпентий-289 имеет чуть больший период распада (87 милисекунд).
Из более-менее стабильных, практически применяемых веществ, самым радиоактивным металлом считается полоний (изотоп полоний-210). Это серебристый белый радиоактивный металл. Хотя его период полураспада достигает 100 и более дней, даже один грамм этого вещества раскаляется до 500°C, а излучение может мгновенно убить человека.
Что такое радиация
Всем известно, что радиация очень опасна и лучше держаться подальше от радиоактивного излучения. С этим трудно поспорить, хотя в реальности мы постоянно подвержены влиянию радиации, где бы не находились. В земле залегает довольно большое количество радиоактивной руды, а из космоса на Землю постоянно прилетают заряженные частицы.
Кратко говоря, радиация это самопроизвольное испускание элементарных частиц. От атомов радиоактивного вещества отделяются протоны и нейтроны, «улетая» во внешнюю среду. Ядро атома при этом постепенно изменяется, превращаясь в другой химический элемент. Когда все нестабильные частицы отделяются от ядра, атом перестает быть радиоактивным. Например, торий-232 в конце своего радиоактивного распада превращается в стабильный свинец.
Наука выделяет 3 основных вида радиоактивного излучения
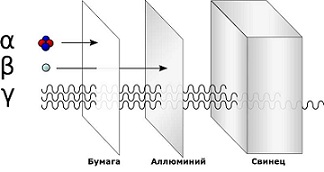
Альфа излучение(α) — поток альфа-частиц, положительно заряженных. Они сравнительно большие по размеру и плохо проходят даже через одежду или бумагу.
Бета излучение(β) — поток бета-частиц, негативно заряженных. Они довольно малы, легко проходят через одежду и проникают внутрь клеток кожи, что наносит большой вред здоровью. Но бета-частицы не проходят через плотные материалы, такие как алюминий.
Гамма излучение(γ) — это высокочастотная электромагнитная радиация. Гамма-лучи не имеют заряда, но содержат очень много энергии. Скопление гамма-частиц излучает яркое свечение. Гамма-частицы проходят даже через плотные материалы, что делает их очень опасными для живых существ. Их останавливают только самые плотные материалы, например, свинец.
Все эти виды излучения так или иначе присутствуют в любой точке планеты. Они не представляют опасности в малых дозах, но при высокой концентрации могут причинить очень серьезный ущерб.
Изучение радиоактивных элементов



Первооткрывателем радиоактивности является Вильгельм Рентген. В 1895 году этот Прусский физик впервые наблюдал радиоактивное излучение. На основе этого открытия был создан знаменитый медицинский прибор, названый в честь ученого.
В 1896 г изучение радиоактивности продолжил Анри Беккерель, он экспериментировал с солями урана.
В 1898 г Пьер Кюри в чистом виде получил первый радиоактивный металл — Радий. Кюри хоть и открыл первый радиоактивный элемент, однако, не успел толком его изучить. И выдающиеся свойства радия привели к быстрой гибели ученого, который беспечно носил свое «детище» в нагрудном кармане. Великое открытие отомстило своему первооткрывателю — Кюри умер в возрасте 47 лет от мощной дозы радиоактивного облучения.
В 1934 г был впервые синтезирован искусственный радиоактивный изотоп.
Сейчас изучением радиоактивности занимаются множество ученых и организаций.
Добыча и синтез



Даже естественные радиоактивные металлы не встречаются в природе в чистом виде. Их синтезируют из урановой руды. Процесс получения чистого металла чрезвычайно трудоемок. Состоит он из нескольких стадий:
- концентрирование (дробление и выделение осадка с ураном в воде);
- выщелачивание – то есть, перевод уранового осадка в раствор;
- выделение чистого урана из полученного раствора;
- перевод урана в твердое состояние.
В итоге, из тонны урановой руды можно получить всего несколько граммов урана.
Синтез искусственных радиоактивных элементов и их изотопов проходит в специальных лабораториях, в которых создаются условия для работы с подобными веществами.
Практическое применение
Чаще всего, радиоактивные металлы используют для выработки энергии.
Ядерные реакторы — это устройства, использующие уран для нагревания воды и создания потока пара, который вращает турбину, с помощью чего вырабатывается электричество.


Вообще, сфера применения радиоактивных элементов довольно широка. Они используются для изучения живых организмов, диагностирования и лечения болезней, выработки энергии и для мониторинга промышленных процессов. Радиоактивные металлы являются основой для создания ядерного оружия — самого разрушительного оружия на планете.
Источник
