Что такое озон и чем он полезен
У этого термина существуют и другие значения, см. Озон (значения).
| Озон | |
|---|---|
| Систематическое наименование | Трикислород |
| Хим. формула | O3 |
| Состояние | голубой газ |
| Молярная масса | 47,998 г/моль |
| Плотность | 0,0021445 г/см3 (г., 0°C); 1,59(7) г/см3 (ж., 85,2 К); 1,73(2) г/см3 (тв., 77,4 К)[1] |
| Поверхностное натяжение | 43,8 Н/м (77,4 К); 38,4 Н/м (90,2 К)[1] Н/м |
| Динамическая вязкость | 4,17 мПа·с (77,6 К); 1,56(2) мПа·с (90,2 К)[1] |
| Энергия ионизации | 12,52 ± 0,01 эВ[3] |
| Температура | |
| • плавления | −197,2 °C |
| • кипения | −111,9 °C |
| Критическая точка | |
| • температура | −12,0 °С (261,1 К)[1] °C |
| • давление | 54,6 атм.[1] |
| Мол. теплоёмк. | 85,354 − 0,2812·(T − 90) (ж., при T от 90 до 160 К)[1] Дж/(моль·К) |
| Энтальпия | |
| • образования | 144,457 (при 0 К, отн. О2)[1] кДж/моль |
| Коэфф. тепл. расширения | 2,0·10−3 К−1 (ж., 90,1 К) 2,5·10−3 К−1 (ж., 161 К)[1] |
| Давление пара | 1 ± 1 атм[3] |
| Растворимость | |
| • в воде | 1,06 г/л (при 0 °С)[2] |
| Диэлектрическая проницаемость | 1,0019 (г), 4,79 (ж)[1] |
| Показатель преломления | 1,0533 (г., 480 нм) 1,0520 (г., 546 нм) 1,0502 (г., 671 нм) 1,2236 (ж., 535 нм) 1,2226 (ж., 589 нм) 1,2213 (ж., 670,5 нм)[1] |
| Дипольный момент | 0,5337 Д |
| Рег. номер CAS | 10028-15-6 |
| PubChem | 24823 |
| Рег. номер EINECS | 233-069-2 |
| SMILES | [O-][O+]=O |
| InChI | InChI=1S/O3/c1-3-2 CBENFWSGALASAD-UHFFFAOYSA-N |
| RTECS | RS8225000 |
| ChEBI | 25812 |
| ChemSpider | 23208 |
| ЛД50 | 4,8 ppm |
| Токсичность | сильнодействующий яд, обладающий раздражающим и канцерогенным действием |
| Пиктограммы СГС | |
| NFPA 704 | 4 4 OX |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
| Медиафайлы на Викискладе | |
Озо́н (от др.-греч. ὄζω — пахну) — состоящая из трёхатомных молекул O3аллотропная модификация кислорода. При нормальных условиях — голубой ядовитый газ. Запах — резкий специфический. При сжижении превращается в жидкость цвета индиго. В твёрдом виде представляет собой тёмно-синие, серые, практически чёрные кристаллы.
Строение озона[править | править код]
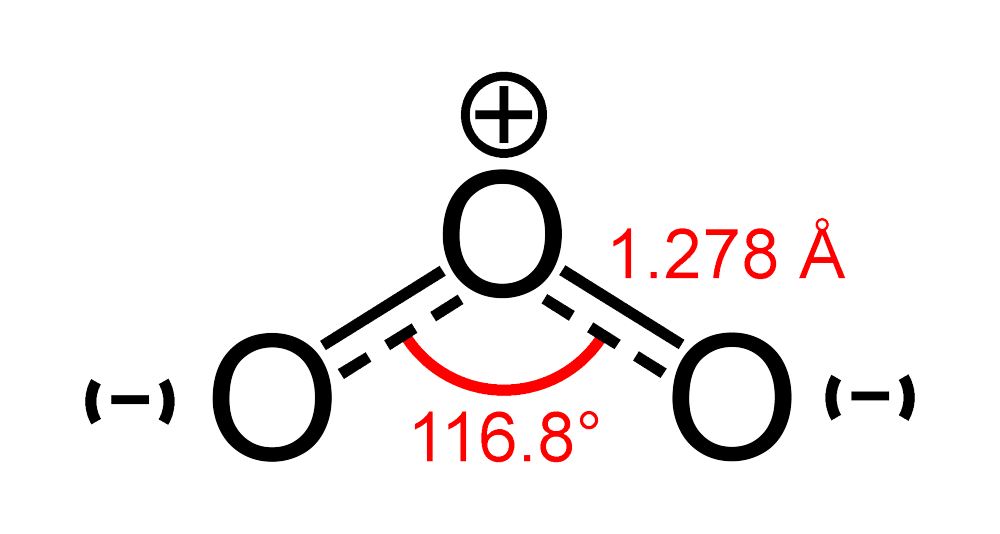
Обе связи O—O в молекуле озона имеют одинаковую длину 1,278 Å. Угол между связями составляет 116,8°[4]. Центральный атом кислорода sp²-гибридизован, имеет одну неподелённую пару электронов. Порядок каждой связи — 1,5, резонансные структуры — с локализованной одинарной связью с одним атомом и двойной — с другим, и наоборот. Молекула полярна, электрический дипольный момент — 0,5337 Д[5].
История открытия[править | править код]
Впервые озон обнаружил в 1785 году голландский физик М. ван Марум по характерному запаху и окислительным свойствам, которые приобретает воздух после пропускания через него электрических искр, а также по способности действовать на ртуть при обыкновенной температуре, вследствие чего она теряет свой блеск и начинает прилипать к стеклу[6]. Однако как новое вещество он описан не был, ван Марум считал, что образуется особая «электрическая материя».
Термин озон был предложен немецким химиком X. Ф. Шёнбейном в 1840 году за его пахучесть, вошёл в словари в конце XIX века. Многие источники именно ему отдают приоритет открытия озона в 1839 году. В 1840 году Шёнбейн показал способность озона вытеснять иод из иодида калия[6]:
Эту реакцию используют для качественного определения озона с помощью фильтровальной бумаги, пропитанной смесью растворов крахмала и иодида калия (иодкрахмальной бумаги) — она в озоне синеет ввиду взаимодействия выделяющегося иода с крахмалом[7].
Факт уменьшения объёма газа при превращении кислорода в озон экспериментально доказали в 1860 году Эндрюс и Тэт при помощи стеклянной трубки с манометром, наполненной чистым кислородом, со впаянными в неё платиновыми проводниками для получения электрического разряда[6].
Физические свойства[править | править код]
- Молекулярная масса — 48 а. е. м.
- Плотность газа при нормальных условиях 2,1445 г/дм³. Относительная плотность газа по кислороду 1,5; по воздуху 1,62 (1,658[8]).
- Плотность жидкости при −188 °C (85,2 К) составляет 1,59(7) г/см³[1].
- Плотность твёрдого озона при −195,7 °С (77,4 К) равна 1,73(2) г/см3[1].
- Температура кипения −111,8(3) °C (161,3 К)[1]. Жидкий озон — тёмно-фиолетового цвета.
- Температура плавления −197,2(2) °С (75,9 К) Приводимая иногда т.пл. −251,4 °C (21,7 К) ошибочна, так как при её определении не учитывалась большая способность озона к переохлаждению[9]. По другим сведениям[1]Tпл = −192,5(4) °С (80,6 К). В твёрдом состоянии — чёрного цвета с фиолетовым отблеском.
- Критическая температура −12,0 °С (261,1 К)[1].
- Критическое давление 51,6 атм[1].
- Коэффициент диффузии (при 300 К, 1 атм) 0,157 см2/с[1].
- Теплота плавления 2,1 кДж/моль[1].
- Теплота испарения при температуре кипения в различных источниках указывается от 11,17 до 15,19 кДж/моль[1]; при 90 К от 15,27 до 16,6 кДж/моль[1].
- Растворимость в воде при 0 °С — 0,394 кг/м³ (0,494 л/кг), она в 10 раз выше по сравнению с кислородом. Кажущаяся растворимость сильно зависит от чистоты воды, поскольку примеси катализируют распад озона.
- Жидкий озон смешивается во всех отношениях с жидкими аргоном, азотом, фтором, метаном, углекислотой, тетрахлоруглеродом. Смешивается с жидким кислородом во всех отношениях при температуре выше 93 К, ниже этой температуры раствор расслаивается на две фазы[1].
- Хорошо растворяется в фреонах, образуя стабильные растворы (используется для хранения и перевозки).
- Потенциал ионизации молекулы 12,52 эВ[1].
- В газообразном состоянии озон диамагнитен, в жидком — слабопарамагнитен.
- Запах — резкий, специфический «металлический» (по Менделееву — «запах раков»). При больших концентрациях напоминает запах хлора. Запах ощутим даже при разбавлении 1:100000.
Химические свойства[править | править код]
Образование озона проходит по обратимой реакции:
Молекула О3 неустойчива и при достаточных концентрациях в воздухе при нормальных условиях самопроизвольно за несколько десятков минут[10] превращается в O2 с выделением тепла. Повышение температуры и понижение давления увеличивают скорость перехода в двухатомное состояние. При больших концентрациях переход может носить взрывной характер. Контакт озона даже с малыми количествами органических веществ, некоторых металлов или их окислов резко ускоряет превращение.
В присутствии небольших количеств азотной кислоты озон стабилизируется, а в герметичных сосудах из стекла, некоторых пластмасс или чистых металлов озон при низких температурах (−78 °С) практически не разлагается.
Озон — мощный окислитель, намного более реакционноспособный, чем двухатомный кислород. Окисляет почти все металлы (за исключением золота, платины[11] и иридия) до их высших степеней окисления. Окисляет многие неметаллы. Продуктом реакции в основном является кислород.
Озон повышает степень окисления оксидов:
Эта реакция сопровождается хемилюминесценцией. Диоксид азота может быть окислен до азотного ангидрида:
Озон не реагирует с молекулярным азотом при комнатной температуре, но при 295°С вступает с ним в реакцию:
Озон реагирует с углеродом при нормальной температуре с образованием диоксида углерода:
Озон не реагирует с аммониевыми солями, но реагирует с аммиаком с образованием нитрата аммония:
Озон реагирует с водородом с образованием воды и кислорода:
Озон реагирует с сульфидами с образованием сульфатов:
С помощью озона можно получить серную кислоту как из элементарной серы, так и из диоксида серы и сероводорода:
В газовой фазе озон взаимодействует с сероводородом с образованием диоксида серы:
В водном растворе проходят две конкурирующие реакции с сероводородом, одна с образованием элементарной серы, другая с образованием серной кислоты:
Все три атома кислорода в озоне могут реагировать по отдельности в реакции хлорида олова с соляной кислотой и озоном:
Обработкой озоном раствора иода в холодной безводной хлорной кислоте может быть получен перхлорат иода(III):
Твёрдый перхлорат нитрония (англ.)русск. может быть получен реакцией газообразных NO2, ClO2 и O3:
Озон может участвовать в реакциях горения, при этом температуры горения выше, чем с двухатомным кислородом:
Озон может вступать в химические реакции и при низких температурах. При 77 K (−196 °C, температура кипения жидкого азота), атомарный водород взаимодействует с озоном с образованием гидропероксидного радикала с димеризацией последнего[12]:
Озон может образовывать неорганические озониды, содержащие анион O3−. Эти соединения взрывоопасны и могут храниться только при низких температурах. Известны озониды всех щелочных металлов (кроме франция). KO3, RbO3 и CsO3 могут быть получены из соответствующих супероксидов:
Озонид калия может быть получен и другим путём из гидроксида калия[13]:
NaO3 и LiO3 могут быть получены действием CsO3 в жидком аммиаке NH3 на ионообменные смолы, содержащие ионы Na+ или Li+[14]:
Обработка озоном раствора кальция в аммиаке приводит к образованию озонида аммония, а не кальция[12]:
Озон может быть использован для удаления железа и марганца из воды с образованием осадка (соответственно гидроксида железа(III) и диоксигидрата марганца), который может быть отделён фильтрованием:
В кислых средах окисление марганца может идти до перманганата.
Озон превращает токсичные цианиды в менее опасные цианаты:
Озон может полностью разлагать мочевину[15] :
Взаимодействие озона с органическими соединениями с активированным или третичным атомом углерода при низких температурах приводит к соответствующим гидротриоксидам. Реакция озона с непредельными соединениями с образованием органических озонидов находит применение в анализе органических веществ.
Получение озона[править | править код]
Озон образуется во многих процессах, сопровождающихся выделением атомарного кислорода, например при разложении перекисей, окислении фосфора и т. п.
В промышленности его получают из воздуха или кислорода в озонаторах действием электрического разряда. Сжижается O3 легче, чем O2, и потому их несложно разделить. Озон для озонотерапии в медицине получают только из чистого кислорода. При облучении воздуха жёстким ультрафиолетовым излучением образуется озон. Тот же процесс протекает в верхних слоях атмосферы, где под действием солнечного излучения образуется и поддерживается озоновый слой.
В лаборатории озон можно получить взаимодействием охлаждённой концентрированной серной кислоты с пероксидом бария[7]:
Токсичность[править | править код]
Высокая окисляющая способность озона и образование во многих реакциях с его участием свободных радикалов кислорода определяют его высокую токсичность. Воздействие озона на организм является общетоксическим, раздражающим, канцерогенным, а также может приводить к преждевременной смерти[16].
Наиболее опасное воздействие высоких концентраций озона в воздухе:
- на органы дыхания прямым раздражением;
Озон в Российской Федерации отнесён к первому, самому высокому классу опасности вредных веществ. Нормативы по озону:
- максимальная разовая предельно допустимая концентрация (ПДК м.р.) в атмосферном воздухе населённых мест 0,16 мг/м³[17];
- среднесуточная предельно допустимая концентрация (ПДК с.с.) в атмосферном воздухе населённых мест 0,03 мг/м³[17];
- предельно допустимая концентрация (ПДК) в воздухе рабочей зоны 0,1 мг/м³.
- Минимальная смертельная концентрация (LC50) — 4,8 ppm
При этом, порог человеческого обоняния приближённо равен 0,01 мг/м³[18].
Озон эффективно уничтожает плесень, бактерии и вирусы.
Применение озона[править | править код]
Применение озона обусловлено его свойствами:
- сильного окисляющего реагента:
- для стерилизации изделий медицинского назначения;
- при получении многих веществ в лабораторной и промышленной практике;
- для отбеливания бумаги;
- для очистки масел.
- сильного дезинфицирующего средства:
- для очистки воды и воздуха от микроорганизмов (озонирование);
- для дезинфекции помещений и одежды;
- для озонирования растворов, применяемых в медицине (как для внутривенного, так и для контактного применения).
Существенными достоинствами озонирования, по сравнению с хлорированием, является отсутствие[18] токсинов (кроме формальдегида) в обработанной воде (тогда как при хлорировании возможно образование существенного количества хлорорганических соединений, многие из которых токсичны, например, диоксин) и лучшая, по сравнению с кислородом, растворимость в воде.
По заявлениям озонотерапевтов, здоровье человека значительно улучшается при лечении озоном (наружно, перорально, внутривенно и экстракорпорально), однако ни одно объективное клиническое исследование не подтвердило сколько-нибудь выраженный терапевтический эффект. Более того, при использовании озона в качестве лекарственного средства (особенно при непосредственном воздействии на кровь пациента) доказанный риск канцерогенного и токсического воздействия перевешивает любые теоретически возможные положительные эффекты, поэтому практически во всех развитых странах озонотерапия не признаётся лекарственным методом, а её применение в частных клиниках возможно исключительно с информированного согласия пациента[19].
В XXI веке многие фирмы начали выпуск так называемых бытовых озонаторов, предназначенных также для дезинфекции помещений (подвалов, комнат после вирусных заболеваний, складов, заражённых бактериями и грибками вещей), зачастую умалчивая о мерах предосторожности, необходимых при применении данной техники[источник не указан 3061 день].
Применение жидкого озона[править | править код]
Давно рассматривается применение озона в качестве высокоэнергетического и вместе с тем экологически чистого окислителя в ракетной технике[20]. Общая химическая энергия, освобождающаяся при реакции сгорания с участием озона, больше, чем для простого кислорода, примерно на одну четверть (719 ккал/кг). Больше будет, соответственно, и удельный импульс. У жидкого озона большая плотность, чем у жидкого кислорода (1,35 и 1,14 г/см3 соответственно), а его температура кипения выше (−112 °C и −183 °C соответственно), поэтому в этом отношении преимущество в качестве окислителя в ракетной технике больше у жидкого озона. Однако препятствием является химическая неустойчивость и взрывоопасность жидкого озона с разложением его на O и O2, при котором возникает движущаяся со скоростью около 2 км/с детонационная волна и развивается разрушающее детонационное давление более 3·107 дин/см2 (3 МПа), что делает применение жидкого озона невозможным при нынешнем уровне техники, за исключением использования устойчивых кислород-озоновых смесей (до 24 % озона). Преимуществом подобной смеси также является больший удельный импульс для водородных двигателей, по сравнению с озон-водородными[21]. На сегодняшний день такие высокоэффективные двигатели, как РД-170, РД-180, РД-191, а также разгонные вакуумные двигатели вышли по УИ на близкие к предельным параметры, и для повышения удельного импульса необходимо найти возможность перейти на новые виды топлива.
Озон в атмосфере[править | править код]
Распределение озона по высоте
Атмосферный (стратосферный) озон является продуктом воздействия солнечного излучения на атмосферный (О2) кислород. Однако тропосферный озон является загрязнителем, который может угрожать здоровью людей и животных, а также повреждает растения.
Считается, что молнии Кататумбо являются крупнейшим одиночным генератором тропосферного озона на Земле.
Примечания[править | править код]
- ↑ 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 Лунин, 1998.
- ↑ Holleman, Wiberg: Lehrbuch der Anorganischen Chemie. ss. 91–100. Auflage. de Gruyter, 1985, S. 460.
- ↑ 1 2 https://www.cdc.gov/niosh/npg/npgd0476.html
- ↑ Takehiko Tanaka; Yonezo Morino. Coriolis interaction and anharmonic potential function of ozone from the microwave spectra in the excited vibrational states // Journal of Molecular Spectroscopy. — 1970. — Vol. 33. — P. 538—551.
- ↑ Kenneth M. Mack; J. S. Muenter. Stark and Zeeman properties of ozone from molecular beam spectroscopy // Journal of Chemical Physics. — 1977. — Vol. 66. — P. 5278—5283.
- ↑ 1 2 3 С. С. Колотов, Д. И. Менделеев. Озон // Энциклопедический словарь Брокгауза и Ефрона : в 86 т. (82 т. и 4 доп.). — СПб., 1890—1907.
- ↑ 1 2 Получение озона и его определение — видеоопыт в Единой коллекции цифровых образовательных ресурсов
- ↑
Справочник химика, т. II. Л., «Химия», 1971. - ↑ Карякин Ю. В., Ангелов И. И. Чистые химические вещества. — М.: Химия, 1974.
- ↑ Earth Science FAQ: Where can I find information about the ozone hole and ozone depletion? Архивировано 1 июня 2006 года.
- ↑ Платина не окисляется озоном, но катализирует его разложение.
- ↑ 1 2 Horvath M., Bilitzky L., & Huttner J., 1985. «Ozone.» pg 44-49
- ↑ Housecroft & Sharpe, «Inorganic Chemistry». — 2005. — P. 439.
- ↑ Housecroft & Sharpe, «Inorganic Chemistry». — 2005. — P. 265
- ↑ Horvath M., Bilitzky L., & Huttner J., 1985. «Ozone.» pg 259, 269—270
- ↑ National Academy of Sciences: Link Between Ozone Air Pollution and Premature Death Confirmed
- ↑ 1 2 Предельно допустимые концентрации (ПДК) загрязняющих веществ в атмосферном воздухе населённых мест. Гигиенические нормативы 2.1.6.1338-03 (недоступная ссылка). Дата обращения 21 ноября 2012. Архивировано 3 декабря 2013 года.
- ↑ 1 2 Озон — мирное оружие XXI века — Костромской научно-исследовательский институт сельского хозяйства
- ↑ Questionable methods of cancer management: hydrogen peroxide and other ‘hyperoxygenation’ therapies Архивная копия от 7 июля 2010 на Wayback Machine, American Cancer Society
- ↑ Перспективные окислители. (недоступная ссылка). Дата обращения 24 декабря 2009. Архивировано 3 ноября 2009 года.
- ↑ The Dynamics of Unsteady Detonation in Ozone
Литература[править | править код]
- Химическая энциклопедия / Редкол.: Кнунянц И.Л. и др.. — М.: Советская энциклопедия, 1992. — Т. 3 (Мед-Пол). — 639 с. — ISBN 5-82270-039-8.
- Разумовский С. Д., Заиков Г. Е. Озон и его реакции с органическими соединениями (кинетика и механизм). — М.: Наука, 1974. — 322 с.
- Лунин В. В., Попович М. П., Ткаченко С. Н. Физическая химия озона. — М.: МГУ, 1998. — 480 с. — ISBN 5-211-03719-7.
Ссылки[править | править код]
- Озон — не всегда хорошо // Наука и жизнь : журнал. — 1992. — № 8. — С. 155.
Источник
ЧТО НАМ ИЗВЕСТНО ОБ ОЗОНЕ С ДЕТСТВА? ОЗОНОВЫЙ СЛОЙ ЗАЩИЩАЕТ ЗЕМЛЮ ОТ УЛЬТРАФИОЛЕТОВОГО ИЗЛУЧЕНИЯ, ХАРАКТЕРНЫЙ ЗАПАХ ЭТОГО БЛЕДНО-ГОЛУБОГО ГАЗА МЫ ЧУВСТВУЕМ ПОСЛЕ ГРОЗЫ. А ЕЩЕ ЕГО ВЫРАБАТЫВАЕТ ОЗОНАТОР – ПРИБОР, КОТОРЫЙ НЕ ТАК ДАВНО ПРИОБРЕЛ ПОПУЛЯРНОСТЬ В СТРАНАХ СНГ. ЧТО ТАКОЕ ОЗОНАТОР И МОЖНО ЛИ ДЫШАТЬ ОЗОНОМ НА САМОМ ДЕЛЕ?
СОДЕРЖАНИЕ:
- Принцип работы озонатора
- Виды озонаторов
- Меры предосторожности при использовании озонатора
- Бытовой озонатор воздуха – польза или вред
- А есть замена озонатору?
Озонатор – это генератор озона, использующийся для устранения запахов и дезинфекции воды и воздуха. Чтобы подробно разобраться в принципе работы этого прибора, начнем с выделяемого им газа. Молекула озона (O3) состоит из молекулы кислорода (О2) и еще одного атома кислорода (О). Атом может отсоединяться от основной молекулы О2 и присоединяться к другим молекулам, изменяя их химический состав. Так в процессе реакции происходит удаление запахов озоном, уничтожение загрязнений, вирусов, бактерий. В дезинфекции O3 гораздо эффективнее хлора, поэтому он и используется для обеззараживания воздуха и воды. Кроме того, считается, что озон избавляет от грибка, плесени и даже пылевых клещей.
Услышав термин «озон», Вы можете подумать об озоновом слое, который защищает нас от опасного ультрафиолетового излучения Солнца. Это озон, который находится в стратосфере. Но есть еще и приземный озон. Озон из приземного слоя является основным компонентом смога в мегаполисах и классифицируется как загрязнитель воздуха. Он создается природой, когда солнечный свет взаимодействует с выделяющимися в окружающую среду химическими веществами, например с выхлопными газами и промышленными выбросами.
Озон является сильным окислителем, поэтому быстро разрушает полимеры, резину, большинство металлов, а также способен выводить из строя электронику. При «передозировке» озона, т.е. превышении максимальной разовой концентрации (она равняется 0,16 мг/м3) озон негативно воздействует на здоровье и может даже привести к отравлению. Признаки отравления озоном: затрудненный вдох, ощущение нехватки воздуха, жжение в груди, кашель, резь в глазах.
Как же использовать озон для обеззараживания?
Дело в концентрации газа: небольшая концентрация не опасна для человека, но по-прежнему справляется с вирусами и бактериями.
Озонирование применяют для:
- стерилизации холодильников, складов;
- обработки воды и воздуха;
- устранения въевшихся неприятных запахов;
- стерилизации медицинских инструментов;
- обеззараживания и увеличения срока хранения продуктов питания;
Также озонирование используется в медицине: озонотерапия применяется для заживления ран, восстановления иммунитета, избавления от целлюлита, ожирения и др. Однако рекомендуем соблюдать осторожность: на наш взгляд, не существует научных доказательств эффективности озонирования для лечения заболеваний. Более того, представители нетрадиционной медицины вводят озон в кровь, суставы и подкожную клетчатку в неизвестных концентрациях, а это крайне небезопасно для здоровья.
ПРИНЦИП РАБОТЫ ОЗОНАТОРА
Грубо говоря, выработка озона в устройстве происходит по принципу грозы. Прибор поглощает кислород из воздуха и придает ему сильный электрический разряд. Этот электрический разряд позволяет кислороду перестраиваться и формировать O3. Затем газ выходит из прибора в воздух или воду. Когда газ вступает в реакцию, то он присоединяется к молекулам загрязняющего вещества и разрушает их структуру.
Озонатор состоит из следующих частей:
- генератор электрических разрядов;
- источник высокого напряжения;
- вентилятор для забора воздуха и подачи озоновой смеси в воду или воздух помещения;
- система автоматического управления.
Для тех, кто хочет не только очистить воздух, но и увлажнить его, предлагают озонатор в комплекте с увлажнителем. В таких устройствах озон обрабатывает воду, залитую в резервуар увлажнителя, так что пар из него выходит уже очищенным. Также в комплектацию некоторых моделей входит ионизатор.
Работа озонатора проходит через следующие этапы:
- Устанавливается время работы (для бытовых озонаторов это, как правило, не более 30 минут) и нажимается кнопка пуска;
- От розетки напряжение идет на генератор электрических разрядов, включается вентилятор и забирает воздух из помещения;
- Образовавшийся в генераторе газ выбрасывается в помещение или емкость с водой;
- Через положенное время прибор отключается автоматически.
ВИДЫ ОЗОНАТОРОВ
По сфере использования выделяют четыре вида приборов:
- Бытовые озонаторы предназначены для небольших помещений и вырабатывают ограниченное количество озона. С их помощью обеззараживают не только воздух и воду, но и продукты питания, мебель, одежду, постельное белье.
- Промышленные модели используют для обработки продуктов питания для выведения пестицидов и химикатов, дезинфекции складов.
- Медицинские озонаторы используются в озонотерапии и для обеззараживания воздуха в медицинских учреждениях.
- Автомобильные устройства работают от бортовой сети автомобиля и используются для дезинфекции машины. По сути они ничем не отличаются от озоногенераторов для дома, разве что их производительность немного меньше.
По назначению есть только два вида устройств:
- Озонаторы воды. При контакте с водой озон активнее уничтожает загрязнения, чем хлор. Однако стоит учитывать, что в результате очистки в воде может образоваться осадок, который необходимо дополнительно обрабатывать, то есть озонирование воды не равно фильтрации.
- Озонаторы воздуха.
МЕРЫ ПРЕДОСТОРОЖНОСТИ ПРИ ИСПОЛЬЗОВАНИИ ОЗОНАТОРА
В первую очередь необходимо проверить, что прибор сертифицирован – это значит, что он прошел проверку на безопасность и соответствие гигиеническим нормативам.
Изучите технические характеристики. Если в инструкции не указаны производительность или максимально допустимое время использования, такое устройство не рекомендуется к использованию.
Прибор опасно включать в помещении с чрезмерно высокой влажностью воздуха и поблизости с взрывоопасными газами или с источником огня.
Не следует нарушать условия эксплуатации, указанные в инструкции, оставлять прибор с открытой крышкой или держать его включенным долгое время. Во время работы озонатора используется высокое напряжение, так что нарушение правил эксплуатации может привести к возгоранию.
Важно! В комнате с работающим озонатором нельзя находиться ни людям, ни домашним животным. После озонирования необходимо тщательно проветрить помещение.
Иногда люди считают, что озонирование и ионизация – это одно и то же. Если кто-то не знает, чем ионизатор отличается от озонатора, поясним: первый прибор насыщает воздух ионами, но в процессе тоже производит озон, концентрация которого зачастую не контролируется и может превышать допустимую норму. Даже в качественно сделанных ионизаторах есть и плюсы, и минусы: отрицательно заряженные ионы притягивают к себе загрязнения, но наряду с этим в ионизированном воздухе быстрее распространяется инфекция.
БЫТОВОЙ ОЗОНАТОР ВОЗДУХА – ПОЛЬЗА ИЛИ ВРЕД
Достоинство озонатора заключается в его способности обеззараживать воду, воздух, продукты питания и многое другое. Прибор удаляет нежелательные запахи, например, запах табачного дыма или готовки.
Под влиянием агрессивной рекламы некоторые смело пользуются озонатором и считают, что у него нет недостатков. Но необходимо помнить, что у озонирования свои нюансы: O3 может быть опасным, если неправильно его использовать.
Назовем некоторые недостатки озонаторов:
- Нет прямых научных доказательств и отзывов авторитетных врачей, что бытовые озонаторы, использующие озон в небольших концентрациях, не превышающих ПДК, удаляют вирусы и загрязнения так же эффективно, как специализированные промышленные озонаторы.
- Озонатор не удаляет из воздуха пыль и пыльцу.
- В воздухе могут находиться примеси, которые, соединяясь с высокой концентрацией озона, могут образовывать токсичные и опасные для человека вещества.
Воздух с большим содержанием озона способен сделать легкие более восприимчивыми к инфекции или повредить дыхательные пути. - O3 может навредить не только Вам, но и растениям и вызвать у них хлороз – состояние, при котором растение не производит достаточное количество хлорофилла.
- Озоногенератор неэффективен против формальдегида и угарного газа.
- Астматики и аллергики наиболее подвержены влиянию озона. В сочетании с пыльцой и другими воздушными аллергенами озон усиливает симптомы аллергии.
- Исследование, проведенное в 2007 году в Медицинском центре университета Дьюка, показало, что вдыхание большого количества озона ослабляет иммунитет. Ученые создали условия для лабораторных мышей, при которых концентрация озона приближалась бы к нездоровой, и обнаружили, что мыши, подвергшиеся воздействию газа, стали более восприимчивы к бактериальным токсинам.
А ЕСТЬ ЗАМЕНА ОЗОНАТОРУ?
Итак, гигантское преимущество озона состоит в том, что он способен крайне эффективно обеззараживать воздух и уничтожать бактерии и инфекции. Но в то же время человеку лучше не контактировать с озоном напрямую. К сожалению, в случае с озонаторами это невозможно – ведь они выпускают озон в воздух вокруг нас.
Но есть приборы, которые обеззараживают воздух и не выпускают озон в комнату.
Один из таких приборов — очиститель-обеззараживатель Tion Clever. Хотя он использует озон для дезинфекции воздуха, он не является озонатором. Отличие в том, что Tion Clever не распространяет озон по помещению. O3 продуцируется внутри прибора, а завершив обработку воздуха, там же, внутри прибора, просто-напросто разлагается до кислорода на специальном фильтре. В комнату попадает очищенный и совершенно безопасный воздух.
Кроме озона, за очистку воздуха в Tion Clever отвечают фильтр первичной очистки от крупной пыли, HEPA фильтр от мельчайших загрязнений и аллергенов, а также АК-фильтр от запахов и вредных газов. Все вместе это обеспечивает фильтрацию воздуха от всех типов загрязнений, включая пыль, пыльцу, шерсть животных и др. Эффективность технологии Tion Clever была подтверждена в “Векторе” – Государственном научном центре вирусологии и биотехнологии. Мы обеспечили медицинским оборудованием с такой же технологией сотни больниц – его эффективность подтверждена научными независимыми статьями.
Между прочим, даже самый чистый воздух не избавит от ощущения духоты, если помещение не проветривать. Две цели – очистка воздуха и проветривание – совмещает бризер, компактная система приточной вентиляции.
Озон может быть как полезен, так и опасен. Как мы выяснили, есть более надежные и эффективные решения для улучшения качества воздуха, чем озонатор. Обеспечить здоровый микроклимат можно с помощью увлажнителя, качественной вентиляции и очистителя-обеззараживателя воздуха. Выбирайте климатическую технику, в безопасности которой Вы уверены.
Источник
